
Actas del Congreso Nacional de
Tecnología Aplicada a Ciencias
de la Salud



Actas del Congreso Nacional de Tecnología Aplicada a Ciencias de la Salud Vol. 1, 2018
Se presenta un modelo funcional de un inyector dual para un prototipo de electro-hilado, el cual procesa membranas porosas por medio de la inyección de dos distintos polímeros (ácido poli láctico y alcohol de polivinilo) y recogidos en un colector para su posterior inyección. Las membranas obtenidas, se aplican como apósitos activos para la regeneración de tejido cutáneo en heridas de segunda intención en ratas de la sepa Wistar. Para ello es necesario un sistema de inyección controlado que pueda regular variables como el flujo de los dos polímeros, pues para cada polímero cambia su viscosidad. Gracias a este dispositivo de control automático, se pueden obtener diferentes morfologías micrométricas de las membranas porosas qué gracias a esta investigación, resultan ser biomateriales que son una promesa como nuevo tratamiento coadyuvante para daños en tejido cutáneo.
Palabras claves: electrohilado, sistema de control, inyección.
A functional model of a dual injector for a prototype of electrospinning is presented, which processes porous membranes by means of the injection of two different polymers (polylactic acid and polyvinyl alcohol) and collected in a collector for subsequent injection. The membranes obtained are applied as active dressings for the regeneration of cutaneous tissue of second intention wounds in rats of the Wistar sepa. This requires a controlled injection system that can regulate variables such as the flow of the two polymers, since for each polymer its viscosity changes. Thanks to this automatic control device, different micrometric morphologies of the porous membranes can be obtained which, thanks to this research, turn out to be biomaterials that are a promise as a new coadjuvant treatment for cutaneous tissue damage.
Key words: electrospinning, control system, injection.
En los últimos años la aplicación de la tecnología hacia otros sectores, como la medicina, textil o alimenticia, ha estado en constante aumento, demandando equipos automatizados para la creación de nuevos materiales. Un ejemplo claro de estos avances es la técnica del “electrospinning” (electro-hilado) que dio inicios en el año de 1902 [1]. Esta técnica consiste en la creación de fibras a escala micrométrica y/o nanométrica que tienen una de sus aplicaciones en el área de la medicina, pues es en esta donde se dan a cabo diversos procesos celulares mediante dichas fibras [2]. La técnica del electro-hilado se efectúa cuando a la solución introducida dentro del equipo es sometida a un alto voltaje [3]. La solución inyectada sobresaldrá en el extremo de una aguja en forma de menisco, el cual se cargará debido a las interacciones electrostáticas. La gota cargada presentará una repulsión electrostática, la cual rompe con la tensión superficial propia de la solución que hará que la gota se estire, generando una geometría cónica (Cono de Taylor); bajo condiciones adecuadas se llega a un punto crítico donde la gota ahora permitirá un flujo constante de la sustancia dando como producto un hilo. Cuando el hilo se dirige hacia un rodillo colector, éste se seca gradualmente. Por efecto del giro de la punta se genera un proceso de batido donde la fibra es finalmente depositada en un rodillo colector, el cual funciona como la tierra del circuito. Para llevar a cabo este proceso es necesario de un sistema de control que realice la inyección de manera uniforme. Éste consta de un motor a pasos, que son ideales para la construcción de mecanismos donde se requieran movimientos muy precisos en el cual necesitará de un driver que aumentará la potencia del motor y le dará sentido de giro al motor. Para regular la velocidad se utilizará un teclado matricial y ésta se visualizará en un LCD. Dependiendo de la viscosidad del polímero se necesitará ajustar la velocidad de inyección a la medida necesaria. También se implementará el uso de un sensor de temperatura para controlarla dentro del electro-hilado y los datos se mostrarán en el display.
El diseño del mecanismo constará de un par de servomotores, los cuales (dado el sentido de giro del motor) girarán a 90° para dar paso a la entrada o salida de la solución, dependiendo de cada jeringa. El objetivo del motor será cambiar su sentido de giro al mismo tiempo que las jeringas cambiarán de estado, pues en un sentido del motor alguna jeringa estará absorbiendo material mientras la otra lo expulsa y cuando el motor cambie de sentido los estados de las jeringas también cambiarán. Esto nos ayudará a realizar una inyección para periodos de tiempo largos donde no hay necesidad de recargar los émbolos que almacenan la solución polimérica. Otra implicación de este sistema de control traerá muchas ventajas en cuanto a las membranas pues se podrá recolectar una mayor cantidad, la cual tendrá una morfología más uniforme.
En el resto del este manuscrito se describe en la sección 2 como fue realizado un control automático para su funcionamiento en continuo y retroalimentación de la solución visco-elástica. Esto incluye monitorear condiciones de temperatura, humedad, drenado y velocidad de inyección durante el proceso, para mejorar las membranas obtenidas. En la sección de resultados se incluye la caracterización de las membranas porosas a base de PVA/PLA, obtenidas mediante procesamiento por “electrospinning”. En la misma sección se presentan los resultados de pruebas de bio-compatibilidad de las membranas porosas poliméricas que incluyen: pruebas in-vitro e in-vivo. Las pruebas in-vitro investigan la adhesión y proliferación celular de fibroblastos dermales de humano. Mientras que las pruebas in-vivo son realizadas en ratas Wistar con heridas de segunda intención. La sección 3 se dedica a las conclusiones de este trabajo de investigación y desarrollo de tecnología para aplicaciones biomédicas.
Inicialmente se cuenta con el proceso de electro-hilado, sin embargo, tras realizar pruebas manuales donde la inyección se realiza mediante una jeringa que se presiona, se llegó a la conclusión de que es necesario un sistema controlado donde la velocidad de inyección sea lo más uniforme posible (ver Figuras 1 y 2). Este fue el planteamiento del problema inicial, lo cual en principio se proponen ideas de los diseños y el sistema de control utilizando engranes y/o cigüeñal, pero se optó por una recolección y vaciado simultaneo, esto gracias a un tornillo sin fin que realiza un movimiento de ida y vuelta (ver Figura 3). La metodología a seguir consta de los siguientes pasos:

Figuras (1) y (2). Aplicación y recolección de las membranas en electro hilado
Primero: se realizó el diseño en SolidWorks el mecanismo deseado. Se propuso la opción de rediseñar el prototipo con un par de guías con el objetivo de que realice el movimiento los más alineado posible.
Segundo: Se imprimieron todas las piezas del mecanismo en una impresora 3D y se probaron materiales para comprobar la resistencia de ellos. Como el objetivo del motor es cambiar el sentido con un movimiento de ida y vuelta, se proporciona en el código esta instrucción de manera que lo pueda hacer tanto manualmente como automáticamente, dependiendo de la necesidad.
Tercero: una vez impresas todas las piezas, se colocaron sobre una base de vidrio (primero se había probado en una base de madera, pero no resultó conveniente debido a los cambios de temperatura y humedad que ésta sufre, la deforman) para que fuera lo más plana posible. Cada pieza se colocó justamente en cada espacio respetando el diseño de SolidWorks.
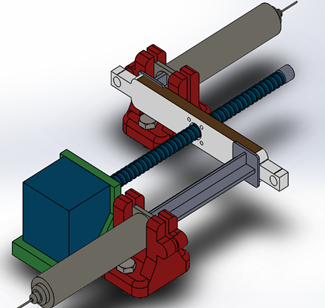
Figura (3). Mecanismo inicial
Durante la programación de los códigos, se implementó algunas opciones posibles, como las diferentes velocidades en cada giro y que éstas se mostraran en una pantalla, también el control de los servos motores se realizó para que pudieran girar sólo 90° para abrir o cerrar las entradas de la llave. El control del sensor de temperatura se integró al microcontrolador, donde también muestra valores en un LCD.
Una vez obtenido el mecanismo que nos ayudará a inyectar el polímero, se prosiguió a realizar una prueba de funcionamiento donde se llenaron las jeringas manualmente y se puso en funcionamiento.
Para la conseguir una solución viscoelástica adecuada se mezclaron dos sustancias principales, PLA y su disolvente natural (cloroformo), en cantidades de: de PLA y de cloroformo, en un vaso de precipitado y calentado a una temperatura de , además de su agitador magnético.
Después de 15 minutos, se verificó que toda la mezcla fuera uniforme y que no quedaran grumos en ella, una vez hecho esto se recolectó toda la sustancia en la jeringa de , para después inyectarla. Se compararon las morfologías de las membranas obtenidas con el inyector y las que se obtuvieron con una inyección manual.
Cuando se realizó el montaje de todas las partes diseñadas en SolidWorks (ver Figuras 4 y 5), se realizó una prueba donde se comprobaba la velocidad de la inyección y se observó que, como era de esperarse, era necesario una velocidad muy baja. Para ello se configuró el tiempo en cada paso, dejando como velocidad apropiada en 2.8 segundos por cada paso. Aquí se mejoró el diseño inicial, integrando un par de guías y un balero en la punta del tornillo del motor (ver Figuras 4 y 5). Una mejora que podría implementarse es la opción de rodamientos lineales (como en las impresoras 3D) en las guías para una mejor movilidad. Además, se realizó una pequeña simulación de todas las partes que lo componen en un simulador para comparar resultados (ver Figura 6). Los datos obtenidos ayudaron a observar los problemas antes de conectar los componentes electrónicos. Este inyector promete obtener una mejor morfología en las membranas además de la inyección controlada y en continuo que se puede obtener. En cada sustancia polimérica ácido poliláctico (PLA) y polivinil alcohol (PVA) cambia su viscosidad. Por lo que el torque necesario para que el motor empuje a ambas jeringas también aumenta, dando como resultado que requiera más corriente eléctrica para trabajar. Como consecuencia el driver del motor sufre calentamiento. Una solución práctica seria incluir un pequeño ventilador al circuito para evitar este efecto.
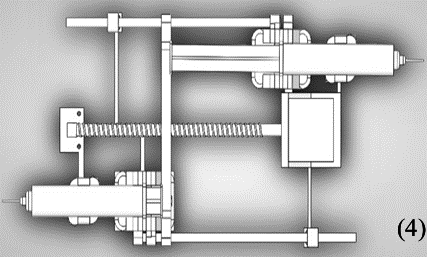

Figura (4). Diseño del inyector en SolidWorks, (5) construcción e impresión de piezas en 3D
Al realizar varias pruebas con los materiales se llegó a la mezcla indicada para conseguir la solución viscoelástica perfecta. Para ello se utilizó de PLA con de cloroformo, pues este último representa un disolvente natural del PLA. Con estas medidas se inyectó a través del electro hilado obteniendo membranas porosas con morfología a escala micrométrica (ver figura 7, 8 y 9).
Durante la creación de las membranas se notaron cambios en la morfología por motivos de la inyección manual. Además, al tener una vibración en el recolector las membranas no presentaban mucha uniformidad, por lo cual se comparó con una inyección con el nuevo sistema y se observó una mejor recolección y uniformidad en el grosor, largo y ancho de la constitución de la membrana.
Las pruebas in-vitro fueron realizadas empleando células de fibroblastos de piel humana. Estos fueron obtenidos por disgregación del tejido cutáneo de un segmento de piel donado y sometido a medio de cultivo celular mezclado con antibiótico para evitar proliferación bacteriana. Posteriormente dicha mezcla fue segmentada y sometida una solución de tripsina al 1X, licuada y filtrada para obtener los fibroblastos. Este tratamiento fue realizado en una autoclave esterilizada a 37 grados centígrados. El resultado fue un cultivo primario celular de fibroblastos mostrado en la figura 10, 11 y 12. Los fibroblastos fueron localizados en la superficie de la membrana y marcados con colorante fluorescente, la cual previamente fue colocada en 18 pozos circulares de 1 milímetro de diámetro por 5 milímetros de altura. En estos pozos se incluyó un control negativo a base de trozos de cobre y un control positivo como medio de cultivo. La finalidad de los controles es para la observación del efecto neto de la membrana sobre los fibroblastos, pues al tener cobre como medio tóxico garantizamos muerte celular en pozos que no tienen membrana, mientras que el control positivo nos permite medir cuanto se reproducen los fibroblastos por efecto del medio de cultivo celular. El comportamiento de los fibroblastos en la membrana fue observado mediante microscopía de fluorescencia hasta después de 24 horas (ver figura 10). El resultado de la observación muestra que los fibroblastos se adhieren, viven y proliferan hasta después de 24 horas. La hipótesis de esto es que la membrana se biodegrada y es absorbida por las células y contribuye a las mismas como alimento.

Figura (7) Micrografía de la membrana sintetizada con el co-polímero ácido poli láctico (PLA) y poli vinil alcohol (PVA); (8) Los diámetros de las fibras son totalmente heterogéneos, sin embrago las fibras del polímero PVA son más gruesos, los cuales se ven más planos; (9) El PLA se muestra más transparente a comparación del polímero PVA.
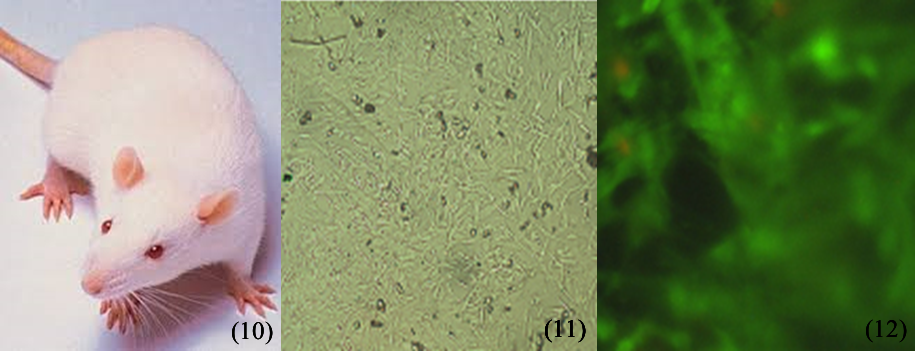
Figura (10) La imagen de la izquierda muestra el bio-modelo sobre el cual se emplearon las pruebas in-vivo; figura (11) se muestra el cultivo de fibroblastos obtenidos de piel humana; figura (12) se muestran los fibroblastos adheridos sobre la membrana de PLA/PVA después de 24 hrs
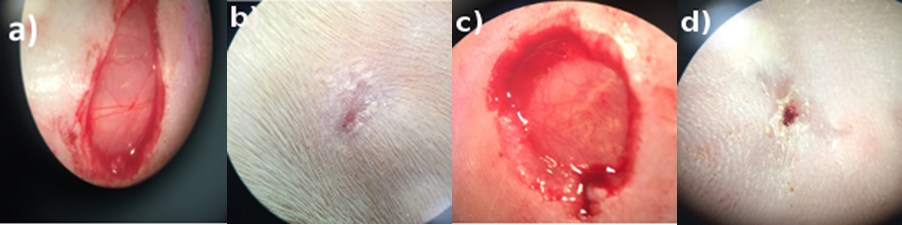
Figura (13): a) Herida de segunda intención, b) la misma que en b) posterior a 15 días con membrana PLA/PVA, c) Control de herida de segunda intención, d) la misma que en c) posterior a 15 días.
Las pruebas in-vivo fueron realizadas en 2 bio-modelos de la cepa Wistar, machos con pesos de 160 gramos aproximadamente, mostrando un ejemplar en la figura (10). El experimento realizado en los bio-modelos, fue realizado según las normas de ética de la norma de experimentos en animales. En el lomo de estos bio-modelos se realizaron 2 heridas de segunda intención en forma ovalada aproximadamente de 0.5 cm de área, hasta alcanzar la fascia muscular, retirando completamente todas las capas de la piel. Previamente les fue suministrada la cantidad necesaria de anestesia a los roedores de acuerdo a su peso. Una herida en los bio-modelos es tomada como control para observar la cicatrización normal, mientras que en la otra herida es colocada la membrana para estudiar su efecto en la herida. A modo de ejemplo se expone la figura (13) con los resultados del proceso de cicatrización en los bio-modelos. Estos resultados muestran que el efecto de la membrana acelera el proceso de cicatrización. La diferencia en el cierre de la herida con membrana y sin membrana es una cicatrización de 3 días. Esto significa que con el uso de la membrana a los 15 días después de realizada la herida, la cicatrización se lleva a cabo completamente, mientras que sin su uso la herida continúa ligeramente abierta al cabo de 15 días. También se observó que la membrana es absorbida por la piel del bio-modelo paulatinamente y el resto de ella es desechado como costra.
Inicialmente el proceso de inyección no contaba con un sistema controlado y esto provocaba chorros en la punta de la jeringa, por lo que se optó en realizar este equipo, tratando de corregir la forma en la que se inyecta el polímero (de PLA o PVA). Inicialmente el inyector demandaba más corriente, pues la entrada de la solución a la jeringa requiere mayor esfuerzo. Cuando se rediseñó el mecanismo incluyendo el par de guías se solucionaron varios problemas de movimiento y fricción, sin embrago éste se puede mejorar. La programación incluyó trabajo adicional, pues se probaron varios códigos y se eligió el de mejor funcionamiento.
Los resultados de las pruebas in-vitro muestran no toxicidad, adhesión y proliferación celular de fibroblastos de piel humana, comprobando que la membrana es un andamio bio-compatible, el cual se bio-degrada y es absorbido por los fibroblastos.
Los resultados de las pruebas in-vivo muestran que la membrana es absorbida por la herida paulatinamente. El efecto neto de esto es una aceleración en la cicatrización de la herida de segunda intención y por ende una reducción en el tiempo de 3 días de la misma. Así que el comportamiento de la membrana es un apósito activo, puesto que cumple con ser bio-compatible y ser degradable por el biomodelo.
Finalmente, el sistema de control ayuda a generar biomateriales en forma de membranas porosas, el cual garantiza un estándar de calidad en el procesamiento de membranas. El uso de estas es como un biomaterial de tercera generación que sirve de andamio celular en el proceso de cicatrización y puede ser un producto médico con uso de apósito activo para regeneración cutánea acelerada.